| Состояние | отпатрулирована |
| Ишемический инсульт | |
|---|---|
 Компьютерная томограмма головного мозга, демонстрирующая инфаркт в правом полушарии головного мозга (зона инфаркта обведена красным.) |
|
| МКБ-10 | I 63 63. |
| МКБ-10-КМ | I63.9 и I63 |
| МКБ-9 | 434.01 434.01 , 434.11 434.11 , 434.91 434.91 |
| МКБ-9-КМ | 433.01 [1] , 433.31 [1] , 434.91 [1] , 433.81 [1] и 433.21 [1] |
| OMIM | 601367 |
| MeSH | D002544 |
Ишеми́ческий инсу́льт — нарушение мозгового кровообращения с повреждением ткани мозга, нарушением его функций вследствие затруднения или прекращения поступления крови к тому или иному отделу. Сопровождается размягчением участка мозговой ткани — инфарктом мозга. Может быть обусловлен недостаточностью кровоснабжения определённого участка головного мозга по причине снижения мозгового кровотока, тромбоза или эмболии, связанных с заболеваниями сосудов, сердца или крови [2] . Является одной из основных причин смертности среди людей [3] .
Содержание
История изучения [ править | править код ]
Первыми сохранившимися упоминаниями инсульта являются описания отца медицины Гиппократа, называвшего заболевание «апоплексия» (греч. ἀποπληξία ) — удар [4] . Теоретические основы по вопросу этиологии инсульта были заложены швейцарским патологом 17-го века Иоганном Якобом Вепфером, обнаружившим, что причиной апоплексии может служить закупорка сосуда головного мозга или сосудистое повреждение с внутримозговым кровоизлиянием [5] . Этим же учёным впервые были описаны клинические случаи очень быстрого регресса слабости в конечностях [6] . Однако окончательно сосудистая природа инсультов была признана лишь в первой половине XIX столетия. «Размягчение» мозга различали от геморрагического «удара», вместе с тем их этиология оставалась до конца неясной. Развитие знаний об инсульте было медленным, по-видимому, в связи с ограниченным интересом у знаменитых неврологов того времени. Так, первые важные сведения о причинах инсульта были получены не неврологами, а патологами Рокитанским и Вирховом [7] . В середине 19-го века хирургом и анатомом Джоном Лиделлом был предложен термин «красный инфаркт», подчёркивающий вторичность кровоизлияния при геморрагическом инфаркте [8] . Клинико-топографические исследования Жюля Дежерина, Пьера Мари, а также их последователя Шарля Фуа — родоначальника современных клинических исследований инсульта, вызвали заинтересованность и дальнейшие исследования неврологов данного заболевания [7] . В 1928 году инсульт был разделён на отдельные типы с учётом характера сосудистой патологии [6] .
Эпидемиология [ править | править код ]
Согласно официальным материалам министерства здравоохранения России за последние годы, смертность от болезней системы кровообращения занимает первое место и при этом продолжает неуклонно расти. В 2002 году вследствие болезней системы кровообращения погибло 56,1 % от общего числа умерших [9] .
Смертность от инсульта находится на втором месте, уступая лишь смертности от ишемической болезни сердца. Суммарные показатели заболеваемости и смертности от инсульта во многих странах мира имеют тенденцию к росту. В России на 2001 год он достиг 331 на 100 тысяч населения [9] .
Ишемические инсульты составляют 70—85 % от всех случаев инсульта, кровоизлияние в мозг — 20—25 %, субарахноидальное кровоизлияние — 5 %. Соотношение частоты ишемических и геморрагических типов инсульта составляет 4:1 [9] .
Классификация [ править | править код ]
Существуют различные классификации ишемических инсультов, в зависимости от этиопатогенетических и клинических аспектов, локализации зоны инфаркта.
По темпу формирования неврологического дефицита и его продолжительности [ править | править код ]
- транзиторные ишемические атаки (ТИА) (G45.9 согласно МКБ-10[10] ) — характеризуются очаговыми неврологическими нарушениями, включая монокулярную слепоту (слепоту на один глаз), которые полностью регрессируют в течение 24 часов после их возникновения [11] :245 .
- «малый инсульт» (англ. minor stroke ) — согласно определению экспертов ВОЗ: «пролонгированные ишемические атаки с обратным неврологическим дефектом». Вариант ишемического инсульта, при котором восстановление неврологических функций завершается от 2 до 21 суток [11] :245 .
- прогрессирующий ишемический инсульт (англ. stroke-in-evolution ) — характеризуется постепенным развитием общемозговых и очаговых симптомов на протяжении нескольких часов или 2—3 суток с последующим неполным восстановлением функций. Обычно у больного остаётся минимальная неврологическая симптоматика [11] :245 .
- завершённый (тотальный) ишемический инсульт — сформировавшийся инфаркт мозга со стабильным или неполно регрессирующим дефицитом [12] .
По тяжести состояния больных [ править | править код ]
- лёгкой степени тяжести — неврологическая симптоматика выражена незначительно, регрессирует в течение 3-х недель заболевания. Вариант малого инсульта [11][12] :247
- средней степени тяжести — преобладание очаговой неврологической симптоматики над общемозговой, отсутствуют расстройства сознания [11][12] :247
- тяжёлый инсульт — протекает с выраженными общемозговыми нарушениями, угнетением сознания, грубым очаговым неврологическим дефицитом, часто дислокационными симптомами[11][12] :247
Патогенетическая (Методические рекомендации по ОНМК, 2000) [ править | править код ]
- атеротромботический инсульт (включая артерио-артериальную эмболию) (34 %) — возникает на фоне атеросклерозацеребральных артерий крупного или среднего калибра. Этот тип инсульта развивается ступенеобразно, с нарастанием симптоматики на протяжении нескольких часов или суток, часто дебютирует во сне. Нередко атеротромботический инсульт предваряется транзиторными ишемическими атаками. Размеры очага ишемического повреждения варьируют [13][14] .
- кардиоэмболический инсульт (22 %) — возникает при полной или частичной закупорке эмболом артерии мозга. Начало кардиоэмболического инсульта, как правило, внезапное, в состоянии бодрствования. В дебюте заболевания наиболее выражен неврологический дефицит. Чаще инсульт локализуется в зоне кровоснабжения средней мозговой артерии, размер очага ишемического повреждения средний или большой, характерен геморрагический компонент. В анамнезе возможны тромбоэмболии других органов [13][14] .
- гемодинамический инсульт (15 %) — обусловлен гемодинамическими факторами — снижением артериального давления (физиологическим, например, во время сна; ортостатической, ятрогенной артериальной гипотензией, гиповолемией) или падением минутного объёма сердца (вследствие ишемии миокарда, выраженной брадикардии и т. д.). Начало гемодинамического инсульта может быть внезапным или ступенеобразным, в покое или активном состоянии пациента. Размеры инфарктов различны, локализация обычно в зоне смежного кровоснабжения (корковая, перивентрикулярная и др.). Гемодинамические инсульты возникают на фоне патологии экстра- и/или интракраниальных артерий (атеросклероз, септальные стенозы артерий, аномалии сосудистой системы мозга) [13][14] .
- лакунарный инсульт (20 %) — обусловлен поражением небольших перфорирующих артерий. Как правило, возникает на фоне повышенного артериального давления. Развивается постепенно, в течение нескольких часов. Локализуются в подкорковых и стволовых структурах (базальных ганглиях, внутренней капсуле, белом веществе семиовального центра, основании моста), размеры очагов не превышают 1,5 см. Общемозговые и менингеальные симптомы отсутствуют, отмечается соответствующая поражённой структуре очаговая симптоматика [13][14][15] .
- инсульт по типу гемореологической микроокклюзии (9 %) (в некоторых источниках также используется термин «реологический инсульт» [16] ) — возникает на фоне отсутствия какого-либо сосудистого или гематологического заболевания установленной этиологии. Причиной инсульта служат выраженные гемореологические изменения, нарушения в системе гемостаза и фибринолиза. Характерна скудная неврологическая симптоматика в сочетании со значительными гемореологическими нарушениями [13][14] .
По локализации инфаркта мозга [ править | править код ]
В соответствии с топической характеристикой очаговой неврологической симптоматики, по пораженному артериальному бассейну [12] :
- внутренняя сонная артерия;
- позвоночные, основная артерия и их ветви;
- средняя, передняя и задняя мозговые артерии.
Факторы риска [ править | править код ]

К основным факторам риска ишемических нарушений мозгового кровообращения относят [16] :232 :
Этиология [ править | править код ]

В качестве локальных этиотропных факторов инсульта различают [19] :
- атеросклероз и тромбообразование — наиболее распространённая патология церебральных и прецеребральных артерий, вызывающая ишемические нарушения мозгового кровообращения. Образование атеросклеротической бляшки обусловлено отложением липидов в стенке артерий. Рост атеросклеротической бляшки осложняется её изъязвлением и тромбообразованием вследствие адгезиитромбоцитов. Увеличение атеротромботической бляшки может привести к сужению просвета артерии и её полной закупорке; снижение кровотока возникает при гемодинамически значимом стенозе (сужение 70—75 % площади просвета) и далее нарастает пропорционально степени сужения. Фрагменты тромба и атеротромботической бляшки могут быть источником эмболии более дистального отдела артерии (артерио-артериальная эмболия). Исход атеросклеротического тромбоза или эмболии определяется скоростью его развития, локализацией закупорки, состоянием коллатерального кровообращения и активностью фибринолитической системы крови. При постепенном развитии атеросклероза формируется коллатеральное кровообращение, поэтому закупорка одной или даже нескольких прецеребральных артерий может не привести к локальной ишемии мозга и протекать бессимптомно. В случаях быстрого развития тромботической окклюзии или эмболии прецеребральной либо церебральной артерии возможности коллатерального кровообращения ограничены. В тех случаях, когда защитные механизмы не могут компенсировать сужение или закупорку артерии, развивается клинически значимая локальная ишемия мозга. Атеротромбоз и артерио-артериальная эмболия являются причиной до 50 % ишемических нарушений мозгового кровообращения [16] :232-233 .
- кардиогенная эмболия является причиной приблизительно 20 % [16] :233 (по некоторым данным до 60 % инсультов обусловлены заболеваниями сердца [19] ) ишемических инсультов и ТИА. Она обычно развивается вследствие формирования эмболических фрагментов на клапанах сердца или образования внутрисердечного тромба. Большинство кардиогенных эмболий возникает при мерцательной аритмии. Она, в свою очередь, обычно вызвана ишемической болезнью сердца на фоне атеросклероза коронарных артерий и артериальной гипертензии. Риск развития инсульта при мерцательной аритмии составляет 4,5 % в год, если больной не принимает соответствующее лечение. При инфекционном эндокардите примерно у 20 % больных возникает эмболия сосудов мозга. Для всех искусственных клапанов сердца общий риск эмболии составляет около 2 % в год, если не принимаются антикоагулянты. Инфаркт миокарда примерно в 2 % случаев осложняется ишемическим инсультом; чаще это происходит первые 2 недели после развития сердечного заболевания [16] :233-234 .
- гемодинамические ишемические нарушения мозгового кровообращения могут возникнуть при стенозе прецеребральных (чаще всего при стенозе сонных артерий) и (или) церебральных артерий, когда артериальное давление падает ниже нижней границы ауторегуляции мозгового кровообращения [16] :234 . Дегенеративные и деформирующие изменения в шейном отделе позвоночника (остеохондроз позвоночника, деформирующий спондилёз, аномалии краниовертебральной области) могут приводить к сдавлению позвоночных или подключичных артерий извне с возможным развитием инсультов в вертебрально-базилярном бассейне [19] либо синдромов обкрадывания[16] :234 .
- редкая сосудистая патология: болезнь Такаясу, Мойамойа, инфекционные артерииты и др.
В качестве системных факторов, способствующих развитию ишемического инсульта, различают:
- нарушение центральной гемодинамики:
- кардиальный гиподинамический синдром — проявляется нарушением кровообращения, сердечного ритма, снижением минутного объёма крови и ударного объёма крови, что приводит к снижению кровотока в артериальной системе мозга, срыву механизмов ауторегуляции мозгового кровообращения и формированию тромботического инсульта или развитию ишемии мозга по типу сосудисто-мозговой недостаточности (гемодинамический инсульт).
- артериальная гипертензия — приводит к развитию ишемических нарушений мозгового кровообращения напрямую, вызывая изменения в стенках артерий — липогиалиноз и фибриноидный некроз, а также опосредованно — через стимулирование атеросклероза прецеребральных крупных и средних церебральных артерий и развитие сердечных заболеваний, например, инфаркта миокарда и мерцательной аритмии, осложняющихся кардиогенной эмболией [16] :232 .
- аритмии — фактор риска возникновения артерио-артериальных и кардиогенных эмболий.
- гематологические нарушения (коагулопатии, эритроцитоз и полицитемия) могут привести к гиперкоагуляции и повышенной вязкости крови, предрасполагающими к развитию тромбозов в церебральных артериях и возникновению «реологического инсульта» [16][19] :235 .
Патогенез [ править | править код ]
Независимо от причины, вызвавшей локальную ишемию мозга, развивается каскад патобиохимических изменений, приводящих к необратимому повреждению нервной ткани по механизмам некроза и апоптоза [16] :235 . Эта серия взаимосвязанных изменений получила название «патобиохимический каскад» или «ишемический каскад» (Гусев Е. И. с соавт.,1997).
Процесс ишемии мозга динамический, и, как правило, потенциально обратимый. Степень ишемического повреждения находится в зависимости от глубины и длительности снижения церебрального кровотока.
Оптимальный объём мозгового кровотока составляет 50—60 мл на 100 г/мин. При уровне церебрального кровотока ниже 55 мл на 100 г вещества в минуту отмечается первичная реакция, которая характеризуется торможением синтеза белков в нейронах — «маргинальная зона ишемии». При церебральном кровотоке ниже 35 мл на 100 г/мин биохимические реакции в клетках мозга нарушаются — гликолиз (расщепление глюкозы) завершается по анаэробному пути с накоплением лактата и образованием всего 2 молекул АТФ. При дальнейшем снижении кровотока возникает нарушение функционального состояния коры большого мозга, а снижение до 10—15 мл на 100 г/мин приводит к быстрым в течение нескольких минут необратимым изменениям в нейронах и формированию центральной зоны инфаркта («ядра ишемии»). В течение 6—8 минут нейроны остаются жизнеспособными и могут восстановить свои функции при нормализации кровообращения.
При локальной ишемии мозга вокруг участка с необратимыми изменениями формируется зона, кровоснабжение которой ниже уровня, необходимого для нормального функционирования, но выше критического порога необратимых изменений — «ишемическая полутень» или «пенумбра» (англ. penumbra ). В этой зоне морфологические изменения отсутствуют. Гибель клеток в области пенумбры приводит к расширению зоны инфаркта. Однако эти клетки в течение определённого времени могут сохранять свою жизнеспособность. Окончательное формирование зоны инфаркта завершается через 48—56 часов [12] [16] :235-236 [19] .
Продолжительность «терапевтического окна» — периода, в течение которого возможно восстановление функции нейронов в области «ишемической полутени» — точно не установлено. Хотя для большинства клеток это время ограничено 3—6 часами, не исключено, что способность к восстановлению сохраняется в течение нескольких суток.
По Скворцовой В. И. (2000 г.), этапами ишемического каскада являются:
Выделяют преходящие нарушения мозгового кровообращения, которые характеризуются регрессом неврологических признаков от нескольких минут до суток после их появления и выделяют острые нарушения мозгового кровообращения со стойкой, часто необратимой симптоматикой в форме инсульта. Инсульты делятся на ишемические и геморрагические.
Ишемический инсульт (инфаркт головного мозга) вызывается значительным снижением кровоснабжения вещества мозга. Макроскопически он определяется четко отграниченной зоной некроза, возникающей в любом отделе головного мозга. Наиболее частая зона поражения – это бассейн средней мозговой артерии.
Различают три наиболее частые причины инфаркта головного мозга:
1. Тромбоз и стенозирующий атеросклероз мозговых артерий. Тромботическая акклюзия чаще возникает в средней мозговой или в соннной артерии. Возможно распространение тромба по внутренней сонной артерии в среднюю и передние мозговые артерии с возникновением инфаркта в обширной части полушария большого мозга.
Атеросклеротическое сужение возможно в любой части сонных и позвоночных артерий.При сужении или закупорке позвоночных артерий ишемические поражения возникают в стволовой части мозга, мозжечке и затылочных долях.
2. Тромбоэмболия в сосуды мозга; источником тромбоэмболии служат пристеночные тромбы, образующиеся в сердце при инфекционном эндокардите, при инфаркте миокарда, при аритмиях, при операциях на венечных артериях или открытом сердце.
3. Поражение артериальной сети мозга местного воспалительного или системного характера: церебральный инфаркт при узелковом периартериите.
Кроме того, церебральные инфаркты могут осложнять заболевания разной этиологии: истинную полицитемию, беременность и послеродовой период, наркоманию, использование некоторых оральных контрацептивов.
Инфаркт мозга подразделяют на белый (бледный, ишемический) и красный (геморрагический). Изменения в ткани мозга в области инфаркта подразделяют на три стадии:
разжижение и начало организации
формирование рубца с полостью или без нее.
Белый инфаркт (серое размягчение головного мозга) при давности процесса менее суток макроскопически определить трудно. В более поздние сроки (3 сутки) – формируется очаг размягчения. Погибшая ткань имеет влажную консистенцию, набухшая, неправильной формы, может прилипать к лезвию ножа. Микроскопически – обнаруживают ишемический некроз нейронов, бледность окраски миэлина, иногда скопление лейкоцитов вокруг погибших сосудов. При обширном повреждении набухание погибшей ткани, отек окружающего мозгового вещества создают повышенное внутричерепное давление, которое может вызвать эффект расширяющегося (объемного) процесса с развитием наружной и внутренней гидроцефалии.
В течение последующих суток ткань в зоне инфаркта подвергается распаду, увлажняется. Особенно четко макроскопическая картина очага размягчения видна на 15 – 21 сутки. Микроскопически в зоне размягчения появляется множество макрофагов («зернистые шары»), заполненных каплями жира и другими включениями (продукты распада миэлина). Перифокально определяются увеличенные астроциты и пролиферация капилляров.
С 21 суток погибшая ткань удаляется и начинается формирование кисты. Через 1 – 1,5 мес. стенка кисты образована атрофичными глиальными и коллагеновыми волокнами с новообразованными сосудами. Вблизи от полости развивается глиоз, видны аксональные шары с петрификацией. Если организуются мелкие инфаркты, то остаются маленькие полости – лакуны.
Красный инфаркт (белый с геморрагическим компонентом) сходен с гематомой, отличием служит сохранение общей архитектоники пораженной ткани. В исходе красного инфаркта макрофаги поглощают гемосидерин, придавая формирующейся кисте бурый цвет.
Смерть при ишемическом инсульте наступает от: 1. Поражения жизненно важных центров; 2. прогрессирующего отека мозга с его дислокацией; 3. присоединившейся пневмонии или тромбоэмболии легочной артерии.
Геморрагический инсульт (церебральная апоплексия) проявляется различными формами спонтанных внутричерепных кровоизлияний.
Внутримозговые кровоизлияния возникают при артериальной гипертонии, при разрыве сосудистой мальформации, при острых лейкозах, при первичных и метастатических опухолях мозга. Внутримозговые кровоизлияния могут быть в форме гематомы или геморрагического пропитывания. Чаще всего они локализуются в зонах базальных ядер, внутренней капсулы, моста мозга и мозжечка.
Морфогенез внутримозговых кровоизлияний. Внутримозговые кровоизлияния развиваются у больных с артериальной гипертонией чаще внезапно в момент повышения артериального давления при физическом или эмоциональном напряжении.
От 1 часа до 12 часов от начала кровоизлияния происходит увеличение объема излившейся крови (формируется гематома).
Первые сутки – в ткани мозга вокруг гематомы развивается отек, полнокровие, стаз, микротромбы, периваскулярные кровоизлияния, выход лейкоцитов, ишемические изменения нейронов.
3 – 4 сутки – вокруг гематомы скапливаются глиальные макрофаги (зернистые шары), гемосидерофаги и развивается глиоз. В результате глиоза начинает формироваться нежная, плохо определяемая капсула («глиальный рубец»). Увеличивающаяся гематома может привести к повышению внутричерепного давления, быстрой деформации мозга, формированию внутренних грыж. Массы излившейся крови способны проливаться в систему желудочков или субэрахноидального пространства.
Для окончательного рассасывания, организации гематомы и образования «апоплексической» кисты необходим длительный, не менее 4 – х недель, период. Апоплексическая киста образуется в результате расщепления и удаления макрофагами гемолизированной крови. Полость кисты заполняется желтой жидкостью.
Другая частая причина спонтанного внутримозгового кровоизлияния – разрыв сосудистой мальформации (порока развития – варикозных расширений вен, артериовенозных аневризм, варьирующих в размерах от мелких капиллярных ангиом до массивных образований, построенных из крупных толстостенных сосудистых каналов).
Субэрахноидальное кровоизлияние (спонтанное нетравматическое) связано с разрывом мешотчатой (в форме ягоды) аневризмы одной из главных мозговых артерий. Мешотчатые аневризмы – врожденные аномалии развития, в основе которых лежит дефект мышечной стенки артерии в зонах ее бифуркации. Диаметр аневризмы 5 – 10 мм, часто они бывают множественными. При разрыве мешотчатой аневризмы кровоизлияние распространяется по субарахноидальному пространству с возможным проникновением масс излившейся крови в вещество мозга и формированием внутримозговой гематомы. При субэрахноидальном кровоизлиянии могут обнаруживаться клинические признаки расширяющегося поражения головного мозга.
Болезни нервной системы
Общее описание
Острое нарушение мозгового кровообращения (ОНМК) по ишемическому типу в бассейне средней мозговой артерии (I65) — это резко возникающая очаговая неврологическая и/или общемозговая симптоматика, обусловленная фокальными ишемическими нарушениями в головном мозге, сохраняющаяся дольше 24 часов.
Распространенность инсультов: 1–4 случая на 1000 человек в год. Ишемический инсульт составляет 70–85% случаев.
Факторы риска: гипертоническая болезнь, нарушение липидного обмена, курение, повышенная масса тела, сахарный диабет, злоупотребление алкоголем, малоподвижный образ жизни.
Острое нарушение мозгового кровообращения происходит в результате атеросклеротического поражения сосудов головы, кардиогенной эмболии при заболеваниях сердца, повышении свертываемости крови и др.
Симптомы острого нарушения мозгового кровообращения
Перед наступлением ОНМК возможно появление предвестников в виде кратковременных неврологических расстройств. В 75% случаев эпизод ишемии происходит во сне. Симптомы появляются на протяжении нескольких минут или часов, постепенно могут нарастать. Характерно повышение артериального давления в первые сутки заболевания. Больных беспокоят следующие жалобы: головная боль (90%), слабость (75%) и/или онемение (70%) в одной половине тела/конечностях, снижение зрения (30%), нарушения речи (45%). 15% пациентов могут отрицать наличие слабости/онемения в конечностях.
При неврологическом осмотре выявляют общемозговой синдром, контралатеральную гемиплегию, гемианестезию, гомонимную гемианопсию, адверсию головы и содружественное отклонение глаз, центральный паралич лица, языка на контралатеральной поражению половине, моторно-сенсорную афазию, алексию, акалькулию. Анозогнозия, расстройство схемы тела определяются при поражении недоминантного полушария.
Диагностика острого нарушения мозгового кровообращения
Для выявления этиологии ОНМК по ишемическому типу необходимы следующие методы диагностики:
- Исследование крови (электролиты, показатели гемостаза, глюкоза, липидный спектр, антифосфолипидные антитела).
- Электрокардиография, измерение артериального давления.
- Аускультация сосудов на конечностях, дуплексное сканирование, транскраниальная допплерография прецеребральных артерий.
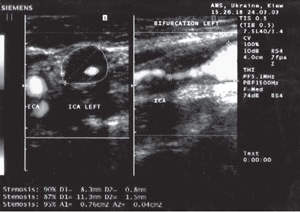 |
| Гипоэхогенная атеросклеротическая бляшка в дистальном отделе правой общей сонной артерии у больного А., 48 лет. |
- Компьютерная томография (КТ) головного мозга — гиподенсивная зона через 12–24 часа от момента развития инсульта по ишемическому типу. ОФЭКТ (на более ранних стадиях ишемии мозга).
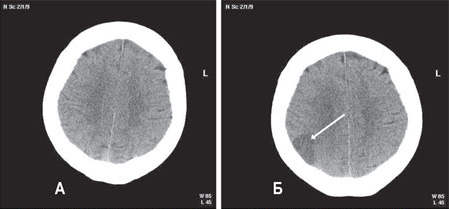 |
| КТ головного мозга больной В., 75 лет, с диагнозом ОНМК по ишемическому типу в бассейне СМА справа: А) КТ при поступлении; Б) КТ на третьи сутки. |
- Церебральная ангиография (стенозы, окклюзии, изъязвления, аневризма).
- Геморрагический инсульт.
- Острая гипертоническая энцефалопатия.
- Дисметаболическая или токсическая энцефалопатия.
- Мигренозный инсульт.
- Черепно-мозговая травма.
- Дебют рассеянного склероза.
Лечение острого нарушения мозгового кровообращения
- Поддержание жизненно важных функций организма, антигипертензивные средства (при артериальном давлении 200/120 мм рт. ст.), антикоагулянты (целесообразность назначения определяется сроком заболевания и сопутствующей патологией), антиагреганты, вазоактивные препараты («Кавинтон», «Актовегин», «Циннаризин», «Инстенон»), нейропротекторы («Церебролизин», «Цераксон», «Пирацетам», «Глиатилин», «Семакс»), «Реополиглюкин», «Трентал», противоотечные средства («Лазикс», «Маннитол»).
- Пассивная ЛФК, дыхательная гимнастика, логопедические занятия.
- Рассмотрение вопроса о тромболизисе при поступлении в срок до 3–6 часов с момента заболевания.
- Реабилитационные мероприятия.
- Вторичная профилактика.
Лечение назначается только после подтверждения диагноза врачом-специалистом.
Основные лекарственные препараты
Имеются противопоказания. Необходима консультация специалиста.

- Гепарин (антикоагулянт). Режим дозирования: в/в или п/к в начальной дозе — в/в (инъекционно) 5000 МЕ, поддерживающая: непрерывная в/в инфузия — 1000–2000 МЕ/ч (20000–40000 МЕ/сут.), предварительно разводя в 1000 мл изотонического раствора NaCl; регулярные в/в инъекции — по 5000–10000 МЕ каждые 4–6 ч; п/к (глубоко) — по 15000–20000 МЕ каждые 12 ч или по 8000–10000 МЕ каждые 8 ч.
- Лазикс (диуретик). Режим дозирования: внутримышечно или внутривенно (медленно струйно) по 20-60 мг 1-2 раза в сутки, в случае необходимости доза может быть увеличена до 120 мг. Препарат вводят в течение 7-10 дней и более, а затем переходят на прием препарата внутрь.
- Пирацетам (ноотропное средство). Режим дозирования: вводится внутримышечно или внутривенно, начиная с 2,0-4,0 г/сут, быстро доводя дозу до 4-6 г/сут. После улучшения состояния дозу снижают и переходят к приему внутрь — 1,2-1,6 г/сут. (0,4 г 3-4 раза в сутки).
- Кавинтон (препарат, улучшающий мозговое кровообращение). Режим дозирования: внутривенно 20-25 мг в 500 мл инфузионного раствора. В течение 2-3 дней дозу можно увеличить не более чем до 1 мг/кг/сутки. Средняя продолжительность курса 10-14 дней. По окончании курса внутривенной терапии рекомендуется продолжить лечение таблетками Кавинтон по 2 таблетки 3 раза в сутки.
- Трентал (сосудорасширяющее, улучшающее микроциркуляцию средство). Режим дозирования: две в/в инфузии в день (утром и днем), в дозе 200 мг (2 амп. по 5 мл) или 300 мг (3 амп. по 5 мл) в 250 мл или 500 мл 0,9% раствора натрия хлорида или раствора Рингера.
Рекомендации
Рекомендуется консультация невролога, КТ головного мозга.