В 1628 году английский врач Уильям Гарвей открыл кровообращение, а спустя некоторое время, в 1661 году, итальянский медик Марчелло Мальпиги — мельчайшие сосудики, капилляры, соединяющие артерии и вены у животных и человека. Сегодня наука о сердечно-сосудистой системе, ее функциях, заболеваниях — одна из ключевых в медицине, однако лишь недавно, в конце ХХ века, ученым пришло в голову, что кровеносные сосуды играют важную роль и в опухолевом росте. Теперь уже никто из медиков не сомневается, что раковая опухоль не может расти без постоянно образующихся вокруг нее новых сосудов.
На протяжении жизни в организме взрослого здорового человека новые кровеносные сосуды и капилляры обычно не образуются. Но после ушиба, пореза, инсульта, ранения и любого другого разрушительного воздействия необходимо восстановить кровоснабжение поврежденных тканей. Вот тогда в организме и «запускается» естественный процесс формирования новых сосудов, называемый ангиогенезом. Во время ангиогенеза эндотелиальные клетки, из которых состоят внутренние стенки сосудов, начинают интенсивно размножаться, и образовавшиеся новые каппиляры прорастают в поврежденные ткани. В организме женщины кровеносные сосуды образуются еще и во время месячного репродуктивного цикла и при беременности.
Хотя post factum многое представляется само собой разумеющимся, но прошло немало лет, прежде чем медики догадались, что для интенсивного размножения опухолевых клеток нужны кислород и питательные вещества, поэтому быстрорастущая злокачественная опухоль требует крови больше, чем, скажем, липома, доброкачественная опухоль из жировой ткани. А значит, по мере развития раковая опухоль должна прорастать новыми кровеносными сосудами .
В 1971 году появилась статья американского хирурга Джуды Фолкмана, в которой впервые было высказано предположение, что рост опухолей, превышающих в диаметре несколько миллиметров, возможен только в случае формирования и прорастания в них мелких капилляров. В 1982 году американские ученые Ваупель, Каллиновски и Окуниефф показали, что во всех злокачественных опухолях действительно идет интенсивное новообразование сосудов. Верно и обратное — если образование новых сосудов прекращается, то дальнейший рост опухоли становится невозможен.
Открытие Фолкмана послужило началом целой череды научных достижений, в результате которых на свет явилась стройная теория ангиогенеза. Согласно ей образование сосудов в раковой опухоли, так же как и в любой поврежденной ткани, протекает в несколько стадий. Что же побуждает организм образовывать новые капилляры?

Американский хирург Джуда Фолкман более 30 лет назад впервые высказал гипотезу о том, что если каким-либо способом прекратить рост сосудов, питающих опухоль, то ее дальнейшее развитие и метастазирование прекратятся.
АКТИВАТОРЫ РОСТА НОВЫХ СОСУДОВ
Оказывается, некоторые ткани организма, да и сами быстрорастущие опухолевые клетки вырабатывают белковые молекулы, стимулирующие прорастание кровеносных капилляров. Такие молекулы называют факторами роста. Самый важный из них — фактор роста эндотелия сосудов (ФРЭС), более известный под английским названием «vascular endothelial growth factor (VEGF)», — выделил в 1989 году французский медик Наполеон Феррара. Сегодня специалистам известна структура гена, отвечающего за синтез этого вещества, а концентрация ФРЭС в опухоли служит диагностическим показателем скорости ее роста (злокачественности). За прошедшие с тех пор почти два десятка лет ученые открыли множество (около 20) сигнальных молекул, стимулирующих образование новых сосудов.
Молекулы факторов роста, в том числе и ФРЭС, связываются на поверхности эндотелиальных клеток, составляющих внутреннюю оболочку сосудов, со специальными белковыми структурами — рецепторами. Рецепторы проявляются под влиянием веществ, которые вырабатывает злокачественная опухоль. На нормальных клетках эндотелия в здоровом организме таких рецепторов нет. Как только молекула ФРЭС связалась с рецептором, инициируется целый каскад биохимических событий: клетки эндотелия начинают интенсивно делиться и «запускают» синтез ферментов — металлопротеаз, которые расщепляют обволакивающий эндотелий внеклеточный матрикс и оболочку сосудов. В образовавшиеся «дырки» эндотелиальные клетки выходят наружу и мигрируют по направлению к опухоли.
Ферменты — металлопротеазы, переваривающие белки, как бы «расплавляют» ткани перед прорастающими сосудами, помогая им продвигаться к цели. Как только кровеносный капилляр окончательно сформировался, активность протеаз падает и ткань вокруг нового сосуда снова «затвердевает». Особенность металлопротеаз состоит в том, что в их активном центре находится атом цинка . Этим опухолевые ферменты отличаются от большинства других природных ферментов, расщепляющих белки, например желудочного пепсина или трипсина поджелудочной железы. Таким образом, ФРЭС и другие факторы роста, взаимодействуя с рецепторами, стимулируют не только рост, но и формирование и продвижение капилляров в глубь опухоли.
Факторы роста совершенно необходимы здоровому организму для восстановления кровотока при различных повреждениях, но их избыток может стать роковым для онкологического больного. Повышение синтеза ФРЭС стимулирует метастазирование опухолей — под воздействием этого вещества раковые клетки выходят в кровяное русло и распространяются по всему организму. С другой стороны, ФРЭС играет и положительную роль — прорастающие в опухоли сосуды формируют в ней своеобразный мягкий скелет, который удерживает клетки на месте, не давая им метастазировать .
Кстати, при недостатке кислорода выработка ФРЭС и других факторов роста усиливается — ведь организму нужно скомпенсировать гипоксию увеличением кровотока. Отсюда можно сделать вывод об увеличении риска онкологических заболеваний при снижении концентрации кислорода в воздухе из-за уничтожения зеленых насаждений, загрязнения окружающей среды и т.д. Также доказано, что молекулы, вырабатывающиеся в организме человека при стрессе, одновременно стимулируют синтез ФРЭС. Этот факт наводит на мысли о пагубной роли нервного напряжения в возникновении раковых опухолей .

ВЕЩЕСТВА, ПРЕПЯТСТВУЮЩИЕ РОСТУ НОВЫХ СОСУДОВ
По счастью, помимо молекул, способствующих прорастанию опухоли сосудами, в организме синтезируются и собственные факторы, препятствующие росту сосудов (ингибиторы). В здоровом организме существует баланс между активаторами и ингибиторами роста новых кровеносных сосудов. При многих серьезных заболеваниях организм как бы теряет контроль над поддержанием этого равновесия. Смещение равновесия в сторону избыточного формирования новых сосудов происходит при онкологических заболеваниях, диабете, ревматоидном артрите и т.д. При таких опасных недугах, как заболевания коронарных артерий, инсульт, напротив, скорость роста новых сосудов явно ниже нормы.
Первым известным природным веществом, тормозящим рост новых сосудов, стал гликопротеин тромбоспондин, вырабатываемый различными клетками, в том числе и клетками стенок кровеносных сосудов. Тромбоспондин тормозит размножение и прикрепляемость эндотелиальных клеток, сдерживая таким путем рост капилляров.
Клиницистам-онкологам давно известно, что первичная опухоль сдерживает рост метастазов. Эффективное подавление или хирургическое удаление первичной опухоли ведет к бурному росту опухолей вторичных. Причина этого явления оставалась неизвестной, пока первооткрыватель роли ангиогенеза в опухолевом росте Фолкман не высказал предположение, что первичная опухоль выделяет какое-то вещество, сдерживающее прорастание сосудов в своих «детках», не давая метастазам расти. Гипотеза блестяще подтвердилась. В 1994 году американец Майкл О’Рейли выделил из мочи мышей с привитой карциномой вещество, которое подавляло рост капилляров. Оно представляет собой фрагмент молекулы содержащегося в крови белка плазминогена. Соединение назвали «ангиостатином» (стабилизирующим сосуды). Оказалось, что при удалении первичной опухоли фактор, сдерживающий рост метастазов, исчезает. В результате вторичные опухоли начинают быстро прорастать новыми сосудами и развиваться. Механизм действия ангиостатина в настоящее время интенсивно изучается.
В 1997 году тот же О’Рейли при исследовании культуры клеток злокачественной опухоли гемангиоэндотелиомы выделил еще один мощный блокатор формирования кровеносных сосудов — эндостатин. Это вещество является частью молекулы полипептида коллагена. Эндостатин активирует программируемую гибель эндотелиальных клеток и, вероятно, тормозит процесс их активации, размножения и миграции.
Помимо тромбоспондина, ангиостатина и эндостатина в органах и тканях животных исследователи обнаружили множество веществ, которые подавляют рост капилляров. К таким веществам относятся некоторые гормоны, фрагменты гепарина и др. Из известных природных ингибиторов можно назвать интерфероны, которые, кстати, борются и с вирусами. Однако как названные вещества, так и многие другие свойственные организму продукты обмена веществ обладают многофункциональным действием и из-за побочных эффектов не могут быть использованы в качестве лекарственных препаратов. Тем не менее интерес ученых к этой группе соединений не ослабевает.
"СОСУДИСТЫЙ" ПОДХОД К ЛЕЧЕНИЮ РАКА
Долгое время противораковая терапия была направлена лишь на подавление роста опухолевых клеток и усиление иммунного ответа. Сейчас уже ясно, что без формирования новых сосудов не может быть роста злокачественных опухолей. Лишенные возможности стимулировать образование новых капилляров, первичные и метастатические опухоли перестают расти. Поэтому появился новый класс ангиостатиков, то есть лекарств, тормозящих прорастание новых кровеносных сосудов. Такие соединения очень перспективны для борьбы со злокачественными опухолями на любой стадии их развития. Более того, существующие сейчас препараты эффективны по отношению к определенным опухолям, а блокаторы роста сосудов могут стать универсальным средством противораковой терапии, причем тем более эффективными, чем злокачественнее опухоль.
Молекулы факторов роста, в том числе и ФРЭС, связываются на поверхности эндотелиальных клеток, составляющих внутреннюю оболочку сосудов, со специальными белковыми структурами — рецепторами. Рецепторы проявляются под влиянием веществ, которые вырабатывает злокачественная опухоль. На нормальных клетках эндотелия в здоровом организме таких рецепторов нет. Как только молекула ФРЭС связалась с рецептором, инициируется целый каскад биохимических событий: клетки эндотелия начинают интенсивно делиться и «запускают» синтез ферментов — металлопротеаз, которые расщепляют обволакивающий эндотелий внеклеточный матрикс и оболочку сосудов. В образовавшиеся «дырки» эндотелиальные клетки выходят наружу и мигрируют по направлению к опухоли.
По противоопухолевой активности другой природный ингибитор — эндостатин сильнее, чем ангиостатин. Уже в малых дозах он предотвращает метастазирование крупных опухолей, а в больших — оказывает мощное тормозящее действие на рост первичных опухолей, таких, как карциномы, саркомы и меланома, вызывая в некоторых случаях их полную гибель. Очевидно, после разработки методов получения ангиостатина и эндостатина в промышленных масштабах эти препараты получат широкое клиническое применение, поскольку существенных побочных реакций при их использовании даже в больших дозах пока не выявлено.
Впрочем, история фармации знает массу примеров, когда вещества, рожденные в пробирке по образу и подобию природных, оказывались и более эффективными, и более безопасными. Если взглянуть назад, то нетрудно убедиться в том, что биологическая и синтетическая химия всегда жили в тесном содружестве. Не «растекаясь мыслью по древу», укажу лишь на то, что первыми противоопухолевыми средствами были природный алкалоид колхицин, выделенный из безвременника подснежного, меркаптопурин — производное пурина, одного из метаболитов нуклеиновых кислот, и эмбихин — полученный модификацией молекулы отравляющего газа иприта, которого в природе нет, и лучше бы и не было . При создании новых лекарственных препаратов ученые работают в трех направлениях: а) получение новых веществ на основе знания молекулярных процессов, в которые требуется вмешаться; б) создание аналогов природных веществ, уже зарекомендовавших себя в клинике; в) скрининг («просеивание через сито») множества веществ, которые просто завалялись на полке и вроде бы должны действовать. Примеры новых ангиостатиков хорошо иллюстрируют эту схему.
Первый класс веществ, которые сейчас испытываются в качестве противоопухолевых препаратов, — соединения, непосредственно блокирующие рост эндотелиальных клеток. К этой категории веществ относится уже упомянутый природный белок эндостатин. Его синтетический аналог комбрестатин А4 — химическая модификация соединения, содержащегося в древесине южноафриканского дерева Combretum caffrum, — проходит клинические испытания. Препарат также проявляет способность подавлять размножение клеток сосудов, стимулируя клеточный апоптоз. В настоящее время большое внимание уделяется созданию веществ, блокирующих размножение уже активированных клеток эндотелия. Из них наиболее удачным по активности и малой токсичности является синтетический препарат TNP-470, прошедший клинические испытания при раке почек, шейки матки и саркоме Капоши.
Ко второй группе препаратов, тормозящих рост сосудов, относятся природные или синтетические вещества, так или иначе блокирующие передачу сигнала на рецепторы факторов роста. Как уже было сказано, ФРЭС взаимодействует с эндотелиальными клетками посредством специальных белковых структур — рецепторов. Клетки здорового организма к этим веществам — блокаторам рецепторов нечувствительны. Клинические испытания проходят препараты антител к ФРЭС, которые эффективно блокируют рецепторы ФРЭС, не давая молекуле фактора роста запустить биохимический каскад, приводящий к прорастанию новых сосудов. Уже понятно, что лекарственные препараты на основе антител замедляют опухолевый рост и продлевают жизнь пациентам. Фактически антитела к ФРЭС — пока единственное антиангиогенное лекарство, уже появившееся на мировом фармацевтическом рынке. Ученые также синтезировали несколько молекул — аналогов ФРЭС, блокирующих рецепторы. Эти вещества тестируются в онкологических клиниках.
На стадии клинических испытаний находится и печально известный препарат талидомид. Почти полвека тому назад он применялся в качестве снотворного, но вызывал уродства плода у беременных женщин. Как случайно выяснилось впоследствии, это было связано с нарушением образования необходимых для роста плода сосудов, хотя механизм действия соединения так и остался до конца не выясненным. Талидомид оказался эффективным при лечении больных миеломой, раком простаты и легких, саркомой и ганглиобластомой.
К третьей группе веществ, подавляющих прорастание сосудов, а следовательно, и рост опухоли, относятся блокаторы (ингибиторы) активности опухолевых ферментов — металлопротеаз, которые разрушают внеклеточный матрикс и оболочку сосуда, давая клеткам эндотелия возможность мигрировать в сторону опухоли. В недавнее время созданы вещества, которые блокируют ионы металлов, входящих в активный центр ферментов, выводя ферменты опухоли из строя и тем лишая ее способности расти. Разработка препаратов такого типа действия — приномастата, маримастата и СOL-3 — находится на стадии клинических испытаний.
Главное достоинство новых препаратов по сравнению с применяемыми в настоящее время состоит том, что они не подавляют размножение других быстрорастущих клеток, например клеток кишечника и крови, но действуют избирательно на опухоли, причем именно злокачественные. Имеет значение и их относительная универсальность. Вещества, подавляющие рост сосудов опухоли, приходят если не на смену, то, во всяком случае, на серьезную помощь известным химиотерапевтическим средствам. На сегодняшний день уже более десяти тысяч пациентов прошли курсы лечения ангиостатиками. Но по-прежнему многие вопросы остаются без ответа — каких побочных эффектов можно ждать от антиангиогенной терапии, как долго может продолжаться курс лечения и не найдут ли опухолевые клетки какой-либо обходной путь, чтобы «опутать себя» кровеносными сосудами? Ответ на них — лишь вопрос времени.
Автор статьи: Доктор медицинских наук В. ПРОЗОРОВСКИЙ
Подпишитесь на НОВОСТИ и получайте эксклюзивную информацию о самых последних исследованиях по противостоянию раку. Информация доступна только подписчикам.
а) Терминология:
• Наличие опухоли или опухолевых клеток в стенке кровеносных сосудов или в их просвете
• Инвазия может быть микроскопической или макроскопической
б) Лучевые признаки прорастания сосудов средостения:
• Рентгенография:
о Объемное образование в легких или средостении центральной локализации
о При рентгенографии оценить инвазию сосудов не представляется возможным
• КТ:
о Дефект наполнения в просвете сосуда, являющийся продолжением опухоли; может накапливать контрастное вещество
о Циркулярный рост опухоли и стенозирование просвета сосуда
о Облитерация просвета сосуда опухолью
о Коллатеральные сосуды при обструкции верхней полой вены
• МРТ:
о Облегчает дифференцирование опухоли с тромбом
о Может выполняться при наличии противопоказаний к внутривенному введению контрастного вещества
• Ангиография:
о Стентирование верхней полой вены при ее обструкции
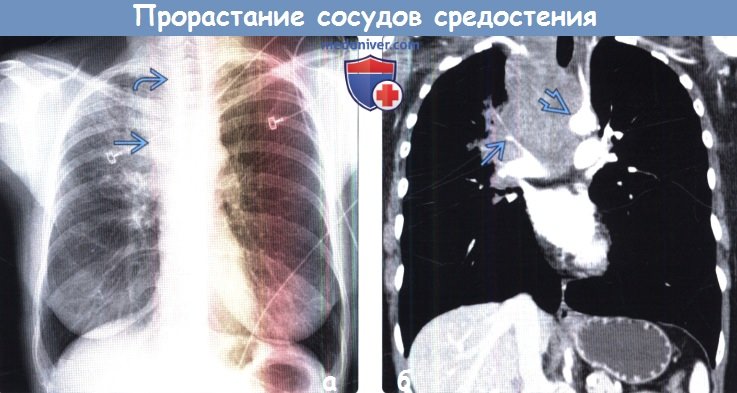 (а) Женщина 52 лет с жалобами на одышку, хрипы и отечность лица в течение трех недель. При рентгенографии органов грудной клетки в ПП проекции в верхней доле правого легкого определяется участок консолидации гетерогенной структуры. Также в правой паратрахеальной области выявляется объемное образование, распространяющееся на область шеи
(а) Женщина 52 лет с жалобами на одышку, хрипы и отечность лица в течение трех недель. При рентгенографии органов грудной клетки в ПП проекции в верхней доле правого легкого определяется участок консолидации гетерогенной структуры. Также в правой паратрахеальной области выявляется объемное образование, распространяющееся на область шеи
(б) У этой же пациентки при КТ с контрастным усилением на реконструкции в коронарной плоскости в средостении визуализируется крупное инфильтративное объемное образование, которое циркулярно прорастает задние отделы дуги аорты правую легочную артерию и ее ветви. КТ с контрастным усилением является методом выбора для оценки инвазии сосудов опухолью. 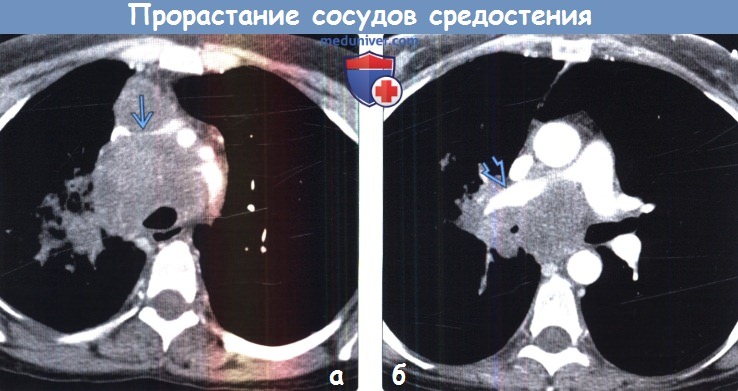 (а) У этой же пациентки при КТ с контрастным усилением в средостении определяется крупное инфильтративное объемное образование, которое циркулярно охватывает левую плечеголовную вену и стенозирует ее просвет. Также выявляется циркулярный рост опухоли вокруг ветвей аорты, возможно, с их инвазией. Следует отметить почти циркулярный охват трахеи опухолью.
(а) У этой же пациентки при КТ с контрастным усилением в средостении определяется крупное инфильтративное объемное образование, которое циркулярно охватывает левую плечеголовную вену и стенозирует ее просвет. Также выявляется циркулярный рост опухоли вокруг ветвей аорты, возможно, с их инвазией. Следует отметить почти циркулярный охват трахеи опухолью.
(б) У этой же пациентки при КТ с контрастным усилением в средостении визуализируется крупное объемное образование, которое циркулярно охватывает правую легочную артерию и стенозирует ее просвет. При биопсии была выявлена низкодифференцированная нейроэндокринная мелкоклеточная карцинома.
в) Дифференциальная диагностика:
• Дефект наполнения в просвете сосуда:
о Артефакт смешивания контрастного вещества, тромб
• Саркома в легочной артерии, в аорте
• Циркулярный рост опухоли вокруг сосуда:
о Ангиоинвазивная грибковая инфекция, медиастинальный фиброз
г) Диагносотические пункты прорастания сосудов средостения:
• КТ с контрастным усилением: метод выбора для оценки инвазии сосуда
• Контакт опухоли с аортой на протяжении >90° ее окружности и отсутствие периаортальной жировой клетчатки свидетельствуют в пользу инвазии
• Инвазию сосуда следует заподозрить при наличии в его просвете дефекта наполнения, являющегося продолжением объемного образования легких/средостения, либо при выявлении циркулярного охвата, окклюзии или облитерации сосуда
• Дефект наполнения в правом предсердии может являться результатом распространения злокачественной опухоли органов брюшной полости через нижнюю полую вену
Редактор: Искандер Милевски. Дата публикации: 13.2.2019
Рак поджелудочной железы — одно из самых коварных и опасных онкологических заболеваний. Он длительное время протекает бессимптомно, а когда дает о себе знать, как правило, оказывается уже инкурабельным. Но даже если диагноз установлен на ранней стадии, пятилетняя выживаемость составляет не более 15%. За счет того, что железа расположена глубоко и окружена другими органами брюшной полости, операции на ней сложны и требуют от хирурга большого мастерства. Высок риск серьезных и подчас фатальных послеоперационных осложнений.
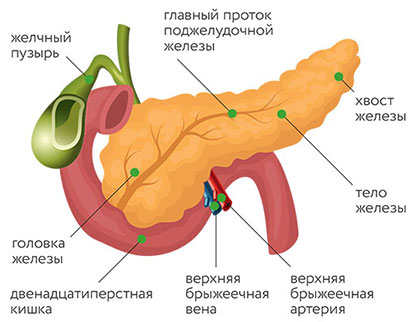
Злокачественная опухоль поджелудочной железы в цифрах и фактах:
- По частоте среди прочих онкологических заболеваний у взрослых занимает шестое место.
- Согласно американской статистике, злокачественные новообразования поджелудочной железы составляют около 3% от всех онкологических заболеваний и обусловливает 7% смертности от всех видов рака.
- Чаще всего опухоль встречается у людей старше 60–65 лет.
- Мужчины и женщины болеют одинаково часто.
- В 50–60% случаев опухоль поражает только головку поджелудочной железы, в 10% — тело, в 6–8% — хвост. В 25–30% случаев поражена вся поджелудочная железа.
Виды рака поджелудочной железы
В поджелудочной железе есть экзокринная ткань, которая вырабатывает пищеварительные ферменты, и эндокринная, функцией которой является производство некоторых гормонов. Соответственно, в зависимости от происхождения, выделяют экзокринные и эндокринные злокачественные опухоли поджелудочной железы. Первые встречаются намного чаще. Когда говорят о раке поджелудочной железы, в большинстве случаев имеют в виду именно экзокринные опухоли.
Аденокарцинома — опухоль из железистых клеток, является самым распространенным типом экзокринного рака. Она встречается в 80–95% случаев. В большинстве случаев опухоль происходит из клеток, выстилающих протоки поджелудочной железы (протоковая аденокарцинома). Реже встречаются новообразования, происходящие из клеток, которые вырабатывают пищеварительные ферменты, в ацинусах. Такой рак называется ацинарно-клеточным.
Отдельно выделяют внутрипротоковые папиллярные и кистозные муцинозные опухоли, ассоциированные с инвазивным раком. Эти новообразования являются доброкачественными, но со временем могут трансформироваться в рак. Люди, у которых диагностированы эти патологии, должны наблюдаться врачом. Кистозные опухоли обычно удаляют хирургически из-за риска озлокачествления. Папиллярные оперируют при определенных условиях, например, если новообразование находится в главном протоке.
Более редкие разновидности злокачественных опухолей поджелудочной железы: плоскоклеточный, недифференцированный, аденосквамозный рак, цистаденокарцинома, перстневидно-клеточная карцинома.
Менее 5% от всех новообразований поджелудочной железы составляют опухоли, которые развиваются из эндокринных клеток (нейроэндокринные опухоли, или опухоли островковых клеток): гастриномы, инсулиномы, глюкагономы, соматостатиномы. Чаще всего они доброкачественные, но могут оказаться злокачественными, причем, даже биопсия не всегда помогает вовремя установить правильный диагноз.
Локализация рака поджелудочной железы
Злокачественная опухоль может находиться в головке, теле или хвосте поджелудочной железы. В зависимости от локализации, она будет иметь некоторые особенности.
Рак головки поджелудочной железы
Чаще всего встречается рак головки поджелудочной железы. Например, здесь локализуется около 75% протоковых аденокарцином. Злокачественные опухоли, удаленные из головки, в среднем имеют размер 2,5–3,5 см, в то время как в теле и хвосте они обычно крупнее. Однако, из-за близкого расположения желчного протока, даже небольшие новообразования головки способны сдавливать его и приводить к механической желтухе. Другие характерные осложнения: стеноз двенадцатиперстной кишки и кровотечение из распадающегося рака.
Рак тела поджелудочной железы
Тело поджелудочной железы — вторая по распространенности локализации рака часть органа. Протоковые аденокарциномы встречаются здесь в 18% случаев. Если опухоль находится в теле или хвосте, то по сравнению с раком головки чаще встречаются такие осложнения, как тромбофлебиты, флеботромбозы, сахарный диабет. Видимо, это связано с тем, что новообразования тела и хвоста имеют более крупные размеры. Если возникает желтуха, обычно это говорит о запущенном раке.
Рак хвоста поджелудочной железы
Рак хвоста поджелудочной железы встречается реже всего. Такую локализацию имеют лишь 7% протоковых аденокарцином. Из-за близости желудка, ободочной кишки и легкого такие опухоли сложнее обнаружить во время УЗИ.

Стадии рака поджелудочной железы
Классификация рака поджелудочной железы по стадиям базируется на общепринятой системе TNM.
Буква T обозначает характеристики первичной опухоли. T1 — опухоль, которая находится в пределах поджелудочной железы, имеет размер до 2 см (T1a) или более (T1b) и не прорастает в капсулу, сосуды, и соседние органы. Стадии T2 и T3 обозначают разную степень прорастания рака в различные структуры.
Буквой N обозначается распространение раковых клеток в лимфатические узлы. N0 — очаги в лимфоузлах отсутствуют. N1,2,3 — распространение рака в различные группы лимфатических узлов.
M — это наличие (M1) или отсутствие (M0) отдаленных метастазов.
В зависимости от сочетаний разных значений T, N и M, рак поджелудочной железы делят на четыре стадии с подстадиями:
T1a
T1b
T2
T3
Рак поджелудочной железы с метастазами
Рак поджелудочной железы с метастазами (стадия IVb), к сожалению, встречается часто: его диагностируют у 45–55% пациентов. Обычно вторичные очаги находятся в различных частях брюшной полости, печени, легких, костях. Радикальное лечение в таких случаях невозможно, но врачи могу купировать боль и другие мучительные симптомы, продлить жизнь больного.
Метастазы в поджелудочной железе
Иногда опухоль, обнаруженная в поджелудочной железе, на самом деле является метастазом рака другого органа. Такое случается редко: метастатический рак составляет лишь 2% от всех злокачественных опухолей поджелудочной железы. Первичная опухоль при этом чаще всего находится в легких, молочной железе, почках, желудочно-кишечном тракте, предстательной железе. Иногда в поджелудочную железу метастазирует меланома, остеосаркома, лейомиосаркома, карцинома Меркеля.
Причины рака поджелудочной железы
Существуют факторы риска, которые провоцируют развитие злокачественных опухолей в поджелудочной железе. Основные из них:
- Сахарный диабет. По неизвестным причинам риск заболевания повышен у людей, страдающих сахарным диабетом второго типа. Риски у больных диабетом первого типа не изучены.
- Желчнокаменная болезнь.
- Хронический панкреатит. Риск особенно высок у курильщиков. Однако, далеко не у всех людей хроническое воспаление в ткани поджелудочной приводит к развитию опухоли.
- Цирроз печени. Есть некоторые доказательства того, что это заболевание становится причиной рака поджелудочной железы.
- Некоторые наследственные факторы: случаи карциномы поджелудочной железы в семье, мутация в гене BRCA2, синдром Линча, синдром множественных диспластических невусов.
- Ассоциированный с меланомой.
- Табакокурение. Один из основных факторов риска. Известно, что около 20–30% случаев онкологии связано с курением сигарет, трубок, сигар.
- Частое употребление алкоголя. Прямая причинно-следственная связь между приемом алкоголя и раком поджелудочной железы не установлена. Но известно, что при частом употреблении спиртного повышается риск хронического панкреатита, цирроза — заболеваний, которые, в свою очередь, являются факторами риска.
- Избыточная масса тела. Установлено, что у тучных людей риск повышен на 20%. Особенно высокую угрозу представляет избыточное отложение жира в области живота, даже если у человека нормальный вес.
- Возраст старше 60–65 лет. Почти всем больным больше 45 лет. Две трети старше 65 лет. Чаще всего заболевание обнаруживают у людей старше 70 лет.
- Кисты и аденомы поджелудочной железы считаются предраковыми заболеваниями.
Можно ли предотвратить рак поджелудочной железы?
Не на все факторы риска можно повлиять, но некоторые эффективные меры профилактики существуют. В первую очередь стоит отказаться от курения — это поможет снизить риск сразу нескольких видов рака. Бросать никогда не поздно, польза для здоровья будет в любом случае. Старайтесь поддерживать здоровый вес, откажитесь от алкоголя – согласно данным некоторых исследований, безопасных доз не существует. Если на работе вам приходится контактировать с вредными химическими веществами, соблюдайте правила безопасности, используйте индивидуальные средства защиты.
Симптомы рака поджелудочной железы
Зачастую первые симптомы появляются уже на поздних стадиях, когда опухоль сдавливает соседние органы, приводит к обтурации (перекрытию просвета) протоков, интоксикации организма продуктами распада.
Боли при раке поджелудочной железы
Первым признаком заболевания, как правило, становится боль. Её появление говорит о том, что опухоль проросла в нервные окончания. Интенсивность болевых ощущений бывает разной, от чувства дискомфорта до острых приступов. Локализация болей зависит от того, какая часть органа поражена:
- головка — под правым ребром;
- хвост — в верхней части живота слева;
- вся поджелудочная железа — боль опоясывающего характера.
Болевые ощущения усиливаются, когда пациент лежит на спине, после приема жирной, острой пищи, алкогольных напитков. Зачастую эти симптомы принимают за проявления панкреатита или других заболеваний, списывают на погрешности в диете и пристрастие к спиртному. Многие люди подолгу не обращаются к врачам, а опухоль тем временем прогрессирует.
Тромбоз
Иногда первым проявлением рака поджелудочной железы является тромбоз глубоких вен ноги. Это состояние проявляется следующими симптомами:
- боль;
- отек;
- покраснение;
- повышение температуры кожи ноги.
Если кусочек тромба оторвется, мигрирует в сосуды легких и перекроет их просвет, развивается осложнение — тромбоэмболия легочной артерии.
Механическая желтуха
Это осложнение развивается, когда опухоль сдавливает желчный проток. Симптомы характерны:
- кожа, слизистые оболочки и склеры глаз становятся желтушными;
- моча темнеет, выглядит как темное пиво;
- стул становится бесцветным;
- живот увеличивается за счет увеличения печени и желчного пузыря;
- беспокоит кожный зуд.
Желтуха нарастает медленно. Сначала кожа имеет ярко-желтый цвет, затем постепенно приобретает зеленоватый оттенок. Со временем развивается почечная и печеночная недостаточность, интенсивные кровотечения, и больной погибает.
Интоксикация
При распаде опухоли в кровь выделяются вещества, которые приводят к интоксикации организма. Возникают следующие симптомы:
- резкая потеря веса;
- снижение аппетита, особенно по отношению к жирной пище, мясу;
- слабость, повышенная утомляемость;
- повышение температуры тела;
- частые депрессии;
- вялость, апатия.
Другие проявления и симптомы
Если опухоль прорастает в кишечник, возникают симптомы кишечной непроходимости. Поражение эндокринных островков приводит к сахарному диабету. При сдавлении селезеночных вен увеличивается в размерах селезенка. Если опухоль прорастает в какой-либо орган, в нем может начаться кровотечение.
Диагностика рака поджелудочной железы
Обнаружить панкреатический рак вовремя, на ранних стадиях, очень сложно. Признаки возникают, когда опухоль успевает прорасти в соседние органы, дать метастазы, и прогноз становится неблагоприятным. Во время осмотра врач может прощупать увеличенную печень, желчный пузырь, селезенку. На более поздних стадиях можно выявить асцит — скопление жидкости в животе.
Все эти признаки неспецифичны, они обнаруживаются и при других заболеваниях.
Обычно при подозрении на рак поджелудочной железы обследование начинают с УЗИ. Это наиболее простой, доступный и недорогой метод диагностики, при этом в большинстве случаев он помогает обнаружить новообразование.
Более информативна эндосонография (эндоУЗИ). Во время этого исследования в двенадцатиперстную кишку вводят специальный зонд, на конце которого находится миниатюрная видеокамера и ультразвуковой датчик. За счет того что датчик подводят максимально близко к поджелудочной железе, он позволяет получить более подробную картину.
Компьютерная томография и МРТ помогают оценить размеры и расположение опухоли, распространение рака на другие органы, выяснить, можно ли удалить новообразование хирургическим путем.
Холангиопанкреатография — исследование, которое помогает оценить состояние протоков поджелудочной железы и желчных протоков. Его можно провести тремя разными способами:
- Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ). Врач вводит в двенадцатиперстную кишку зонд, находит отверстие, через которое впадает желчный проток, и вводит через него рентгеноконтрастное вещество. Затем проводят рентгенографию: «прокрашенные» протоки становятся хорошо видны на снимках.
- Чрескожная чреспеченочная холангиография показана, если не удается провести ЭРХПГ. Рентгеноконтрастное вещество при этом вводят через иглу.
- Магнитно-резонансная холангиопанкреатография (МРХПГ) — это по сути обычная магнитно-резонансная томография. Это неинвазивное исследование, в организм пациента не нужно вводить инструменты. Но во время МРХПГ, в отличие от ЭРХПГ, невозможно провести биопсию, выполнить лечебные манипуляции.
Биопсия — исследование образца ткани поджелудочной железы под микроскопом. Это самый точный метод диагностики в онкологии, он помогает окончательно подтвердить или исключить наличие раковых клеток.

Для того чтобы разобраться, можно ли выполнить радикальную операцию, зачастую приходится проводить ангиографию. Это рентгенографическое исследование, во время которого кровеносные сосуды «прокрашивают» с помощью контрастного раствора.
ПЭТ-сканирование помогает обнаружить отдаленные метастазы.
В биохимическом анализе крови при раке поджелудочной железы обнаруживают повышение уровней ферментов (амилаза, липаза и др.), билирубина, печеночных трансаминаз (АлАт, АсАт), желчных кислот. В запущенных случаях снижается уровень белка.
Рак поджелудочной: код по МКБ-10
В Международной классификации болезней десятого пересмотра (МКБ-10) раку поджелудочной железы присвоен код C25 — «злокачественные новообразования поджелудочной железы». В нем выделяют восемь уточняющих диагнозов — подрубрик:
- C25.0 — опухоли головки поджелудочной железы;
- C25.1 — злокачественные образования тела поджелудочной железы;
- C25.2 — опухоли хвоста поджелудочной железы;
- C25.3 — опухоли протока поджелудочной железы;
- C25.4 — новообразования из островковых клеток;
- C25.7 — опухоли других частей органа;
- C25.8 — опухолевое поражение нескольких частей, перечисленных выше;
- C25.9 — неуточненное опухолевое поражение поджелудочной железы.
Лечение рака поджелудочной железы
Так как заболевание чаще всего диагностируют на поздних стадиях, его лечение представляет собой большую проблему. Прибегают к хирургическим методам, лучевой терапии, химиотерапии, гормональной терапии.
Хирургическое лечение
Хирургическое удаление опухоли возможно только в 10–15% случаев. При этом должны быть соблюдены три условия:
- панкреатический рак не должен прорастать в соседние органы;
- не должно быть метастазов;
- здоровье пациента должно позволять перенести серьезную операцию (поэтому хирургическое лечение чаще проводят у молодых людей).

Во время операции удаляют часть поджелудочной железы или всю её целиком, иногда с частью двенадцатиперстной кишки, желудка, общего желчного протока, ближайшими лимфатическими узлами, если они поражены опухолевым процессом. Чаще всего приходится прибегать к операции Уиппла — панкреатодуоденальной резекции.
В Европейской клинике работают опытные хирурги и функционирует превосходно оснащенная операционная. Мы выполняем операции любой сложности.
В некоторых случаях между желчным пузырем и тощей кишкой хирургическим путем устанавливают анастомоз, который обеспечивает прямой отток желчи. Когда опухоль невозможно удалить из-за глубокого прорастания, врачи прибегают к выполнению ряда манипуляций, облегчающих выведение желчи и улучшающих самочувствие пациента.
После радикального лечения пациент должен пожизненно принимать ферменты и препараты инсулина.
Рак поджелудочной железы растет очень быстро. Если радикальное лечение невозможно, удалять часть опухоли нецелесообразно, особенно у людей старшего возраста, страдающих сопутствующими заболеваниями. Риски серьезного хирургического вмешательства сильно перевешивают потенциальную пользу.
Одно из самых распространенных и серьезных осложнений рака поджелудочной железы — механическая желтуха. Для того чтобы восстановить отток желчи, прибегают к паллиативным вмешательствам:
- Наложение анастомоза между тощей кишкой и желчным пузырем.
- Установка дренирующего катетера во время эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ). Периодически катетер засоряется, через каждые 3–4 месяца его нужно менять.
- Установка стента (жесткого металлического каркаса с сетчатой стенкой, который расширяет просвет протока) во время чрескожной чреспеченочной холангиографии.
Химиотерапия

Химиопрепараты при раке поджелудочной железы имеют слабый эффект. Чаще всего их назначают в сочетании с лучевой терапией, особенно при неоперабельных опухолях, чтобы продлить жизнь и улучшить самочувствие пациента.
Хорошие результаты показывает гормональная терапия, так как на опухолевых клетках в поджелудочной железе часто присутствуют рецепторы к эстрогенам, которые стимулируют их рост. В ряде случаев гормональные препараты помогают продлить жизнь больного.
Лучевая терапия при раке поджелудочной железы
Чаще всего лучевую терапию назначают после операции, чтобы убить оставшиеся в организме раковые клетки. Иногда назначают курс предоперационной (неоадъювантной) лучевой терапии, чтобы облегчить удаление опухоли. При неоперабельном раке лучевая терапия может стать основным методом лечения, она помогает избавить пациента от болей.
Питание при раке поджелудочной железы
У многих людей, страдающих раком поджелудочной железы, нарушается питание. Из-за этого они сильно теряют вес, постоянно испытывают слабость, развивается анемия и другие осложнения. Поэтому всегда важно оценивать нутритивный статус таких больных и проводить его коррекцию. Питание должно быть максимально полноценным, с учетом физиологических возможностей пациента.
Многие больные должны регулярно принимать панкреатические ферменты в виде таблеток. Если человек не может полноценно питаться самостоятельно, его кормление осуществляется через назогастральный зонд — тонкий катетер, введенный через нос в желудок.
Рак поджелудочной железы: прогноз по сроку жизни
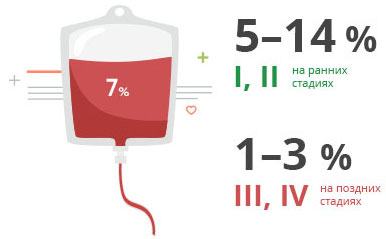
Панкреатический рак отличается относительно низкими показателями пятилетней выживаемости. На ранних стадиях они составляют 5–14%, на поздних — 1–3%.
Даже если рак диагностирован поздно, и прогноз однозначно неблагоприятный, это еще не означает, что пациенту ничем нельзя помочь. Врачи Европейской клиники знают, как снять боль и другие мучительные симптомы, продлить жизнь, обеспечить её достойное качество. Мы беремся за лечение рака поджелудочной железы на любых стадиях.